北九州市立病院機構・臨床研究推進センターのホームページをご覧いただきありがとうございます。
恐らく、このページをご確認いただいているということは、治験、臨床研究について興味がある、若しくは、ご自身や家族、友人等の健康上の理由により、高度で質の高い医療に関心があり、そのような医療を受診したいと思っておられるのかもしれません。
しかしながら、これまでに治験や臨床研究という言葉を聞いたことがあっても、各種制度上の違い、具体的な内容、関わり方など、詳しくは分からないという方も多いのではないでしょうか。
臨床研究推進センターでは、治験・臨床研究に関する様々な情報発信による啓発活動を通して、北九州市域のより多くの方々に、臨床研究のことを知っていただき、先進的な医療が受けられる環境を整えていきたいと考えています。
治験や臨床研究は、医学研究の枠組みの中で取り扱われています。医学研究には、広く動物実験や、遺伝子組み換え実験なども含まれますが、人を対象とする研究になると様々な法律や倫理指針のもと厳正に管理のうえ実施しなければならなくなります。
主な枠組みについては、以下に示すとおりです。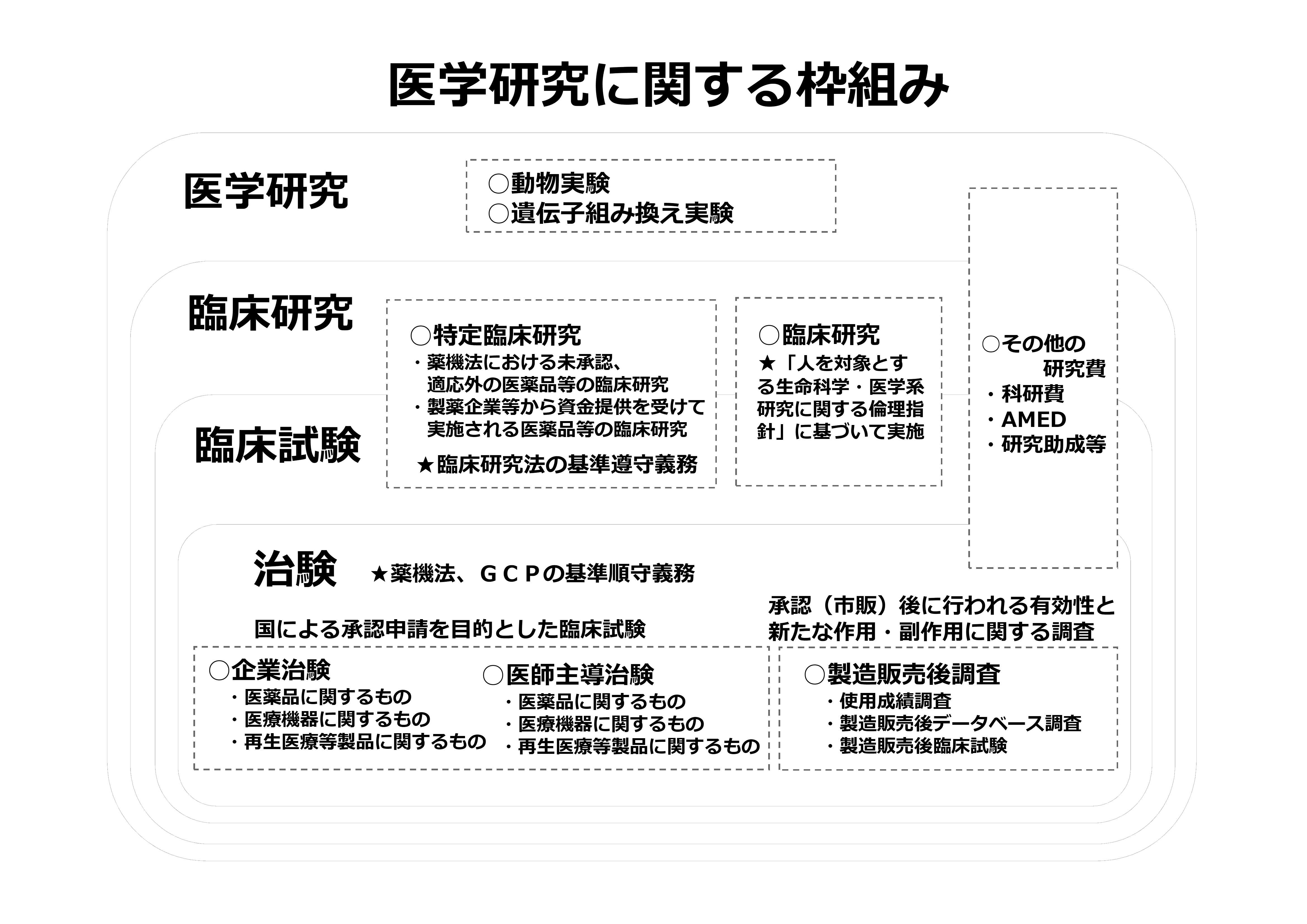
臨床試験のうち、薬や医療機器の使用に関して、国による承認申請を目的として行われるものを治験といいます。具体的には、例えば「薬の候補」となる物質について、製薬会社や医療機関等がその効果や安全性、治療法などを確認します(治験)。その結果を国(厚生労働省)に申請し、国の承認が得られた場合にはじめて、薬が一般的な治療法として使用されるようになります。
国の承認を得る手続きとなる訳ですから、治験を実施するにあたっては、「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)」や「医薬品の臨床試験の実施の基準に関する省令(GCP(Good Clinical Practice))」など様々なルールのもと行う必要があります。
詳細については、厚生労働省のホームページををご参照ください。治験に関する厚生労働省ホームページ[外部リンク]
治験には、企業(製薬会社等)が主導して行われるもの(企業治験)、医師が主導して行われるもの(医師主導治験)があります。また、国の承認後に販売された医薬品や医療機器の安全性や有効性を確認するために行われる市販後(製造販売後)調査、と呼ばれるものがあります。

